Работа с органическими растворителями. Источники опасности
20-12-2011, 20:07. Разместил: Admin
Работа с органическими растворителями. Источники опасности
Особое место среди применяемых в лабораториях огнеопасных веществ занимают органические растворители. Они легко воспламеняются, быстро горят и с трудом тушатся. При горении ЛВЖ- выделяют теплоту в 10 раз интенсивнее, чем древесина. Пары многих органических растворителей даже при комнатной температуре способны образовывать с воздухом пожаро-взрывоопасные смеси. Опасность применения и хранения органических растворителей зависит от ряда условий — количества и горючести жидкости, температуры, герметичности аппаратуры или тары, наличия источников воспламенения и т. д.
К 1 разряду относятся: акролеин, адлилхлорид, ацеталь, ацетальдегнд, ацетон, бензины, гексан, диметилдихлорсилан, дйпро-пиловый эфир, диэтиламин, днэтиловый эфир, нзопропиламин, изо: пропилхлорид, метилаль, метилметакрилат, метилформиат, пропн-леноксид, петролейный эфир, пропилхлорид, сероуглерод, .тетрагидрофуран, фуран, циклогексан, циклогексен, этнламин, этилформиат и др.
К 2 разряду относятся: акрилонитрил, аллилбромид, аллил-амин, амилхлорид, ацетонитрил, бензол, бутиламин, 2-метил-пропанол, бутилхлорид, винилацетат, гексаметилдисилоксан, тептан, дибутиловый эфир, диоксан, дихлорэтан, диэтилхлорсилан, диэтил-кетон, изопропилацетат, изопропилформиат, изопропил-карбонат, лигроин, метилацетат, метанол, метилтрихлорсилан, метил-хлорформиат, метилэтилкетон, пиперидин, пиридин, толуол, триэтил-амин, циклогексиламин, этилакрилат, этилацётат, этилбензол, этилен-имин, этанол и др.
К 3 разряду относятся: амилацетат, амилбромид, амил-формиат, анизол, ацетилацетон, бензилхлорид, бромбенэол, бутанол, гексилхлорид, декан, диамиловый эфир, дикетен, диметиламиноэтанол, диметилсульфат, М,М-диэтиламиноэтанол, диэтилкарбонат, изоамилацетат, керосины, ксилол, метилакрилат, морфолин, муравьиная кислота, октиламин, пентанол, пропилбензол, пропанол, скипидар, стирол, уайт-спирит, уксусная кислота, уксусный ангидрид, хлорбензол, циклогексанон и др.
Жидкости, имеющие температуру вспышки выше 61 °С в закрытом тигле или выше 66 °С в открытом тигле и способные гореть после удаления источника зажигания, относятся к ГЖ.
Образование пероксидов. Некоторые органические растворители в процессе хранения способны поглощать кислород воздуха и реагировать с ним, образуя пероксиды. Органические перокси-ды представляют собой нестабильные соединения, разлагающиеся под действием удара, трения, тепла, пламени, загрязнений, а иногда и без видимых причин. Опасность применения растворителей, содержащих пероксиды, связана прежде всего с тем, что в определенных условиях разложение может происходить очень бурно и даже со взрывом.
Особенно велика опасность взрыва при перегонке или упаривании жидкости, содержащей пероксид. Как правило, пероксиды обладают меньшей летучестью по сравнению с исходным растворителем, и во время перегонки концентрация их в кубе увеличивается. При попытке отогнать растворитель досуха может произойти взрыв.

Некоторые жидкости при неблагоприятных условиях хранения способны накапливать пероксиды в таких количествах, когда вероятность взрыва возникает даже без упаривания растворителя. Автору известен случай самопроизвольного взрыва тетрагидрофураиа, хранившегося более года над гранулированной щелочью в литровой бутылке под корковой пробкой. Взрыв произошел через 10—15 мин после того как бутылку принесли с мороза в теплое помещение. «
Иногда взрывы могут быть следствием бурного взаимодействия пероксидов с теми или иными реагентами. Так, например, небезопасно добавление гранулированной щелочи к содержащим пероксиды тетрагидро-фурану или диоксану с целью их осушки.
Вследствие способности связи —О—О— к гомоли-тическому расщеплению с образованием двух радикалов пероксиды инициируют радикальные реакции. В случае применения растворителей,,содержащих пероксиды, возможно непредусмотренное течение реакции, по радикальному, механизму, которое иногда сопровождается сильным экзотермическим эффектом. Инициируемой пероксидами экзотермической полимеризации подвержены такие соединения, как метилметакрилат, стирол, акриловая .кислота, акрилонитрил, бутадиен, винилиденхлорид, тетрафторэтилен, хлортрифторэти-лен, винилацетилен, винилхлорид, винилпиридин, хлоропрен и др. При длительном контакте перечисленных соединений с кислородом воздуха в отсутствие инигибвторов образуется достаточное для инициирования полимеризации количество пероксида.
Работа с легковоспламеняющимися жидкостями
При работе с ЛВЖ следует придерживаться трех основных принципов:
- не допускать попадания горючих паров в атмосферу (предотвращать образование пожаровзрывоопасных смесей);
- исключать возможность воспламенения при случайном образовании пожаровзрывоопаснон концентра -ции паров (исключать возникновение источников зажигания) ;
- заранее принимать все возможные меры, чтобы последствия аварии, если она все же произойдет, были минимальными.
Таблица 4. Степень утяжеления воздуха насыщенными парами некоторых жидкостей при 20° С
Жидкость |
Молекулярная масса |
Температура кипения, °С |
Давление насыщенного пара, мш рт. ст. |
Концентрация в воздухе, мг/л |
Степень утяжеления воз-Духа, % |
Диэтиловый эфир |
74,12 |
35,6 |
442,0 |
1795 |
90 |
Сероуглерод |
76,14 |
46,3 |
292,0 |
1200 |
63 |
Хлороформ |
119,37 |
61,2 |
159,6 |
1080 |
65 |
Четыреххлористый углерод |
153,81 |
76,8 |
91,0 |
764 |
51 |
Бензол |
78,12 |
80„1 |
75,1 |
320 |
17 |
Хлорбензол |
112,50 |
132,1 |
8,8 |
53 |
3 |
Уксусный ангидрид |
102,09 |
140,0 - |
2,7 |
15 |
0,9 |
Анилин |
93,13 |
184,4 |
0,4 |
2;0 |
0,5 |
Нитробензол |
123,11 |
210,9 |
0,26 |
1,7 |
0,3 |
Ртуть |
200,59 |
356,9 |
0,0012 |
0,0143 |
0,1 |
Хранение и проливы ЛВЖ- Пары ЛВЖ могут попадать в атмосферу при несоблюдении температурных режимов хранения или при хранении их в негерметично закрытой таре. Концентрация паров ЛВЖ в воздушном пространстве внутри тары всегда выше верхнего концентрационного предела воспламенения (ВКПВ) для жидкостей I разряда и выше и близка к ВКПВ для жидкостей II разряда. При выходе из горловины через неплотности в укупорке пары разбавляются воздухом, и в некотором объеме рядом с емкостью образуется зона взрывоопасных концентраций. Поскольку пары этих жидкостей тяжелее воздуха, при отсутствии вентиляции они могут скапливаться в нижних частях складских помещений, что создает условия для длительного сохранения опасной обстановки.

В лабораторных помещениях не допускается хранение даже небольших количеств ЛВЖ с температурой кипения ниже 50 °С (пентан, сероуглерод, диэтиловый эфир). В конце рабочего дня остатки таких растворителей следует вынести в специальное холодное помещение (см. разд. 1.4). Хранение прочих ЛВЖ, в соответствии с нормами, утвержденными руководителем организации, допускается в толстостенных бутылках вместимостью не более 1 л, снабженных герметичными пробками. Бутылки с ЛВЖ помещают в специальные металлические ящики, установленные вдали от источников тепла. Запрещается выливать отходы ЛВЖ в канализацию.
Особую опасность представляет пролив ЛВЖ в лабораторных помещениях. Хотя полностью предотвратить возможность пролива по неловкости невозможно, следует принимать меры, чтобы свести вероятность пролива к минимуму и ограничить количество жидкости, которое может пролиться.
В лабораторию жидкости- следует доставлять в плотно закрытых бутылках вместимостью не более 1 л, помещенных в специальную металлическую корзину с ручками. Расфасовку ЛВЖ из больших бутылей производят в специально оборудованных подсобных помещениях (см. разд: 1.4). Под приборы, содержащие более 0,5 л ЛВЖ, необходимо помещать кювету, чтобы в случае аварии ограничить площадь растекания жидкости. При необходимости хранения ЛВЖ в тонкостенных емкостях (ампулы, сосуды Шленка) их следует помещать в металлические контейнеры или фарфоровые стаканы, заполненные на 4—5 см песком или асбестовой крошкой.
Одной из причин разрушения стеклянной тары могут послужить температурные колебания окружающей среды. Необходимо строго следить, чтобы емкости с ЛВЖ не оказались рядом с нагретыми предметами и не освещались прямыми лучами солнца. При температуре 58 °С внутри герметично закрытой емкости с пента.г ном создается давление, в 2 раза превышающее атмосферное, что может вызвать разрушение стеклянных бутылок, имеющих механические повреждения. Для этилового эфира такое же избыточное давление достигается при 56 °С, для метилформиата — при 51,9 °С, для трихлорфторметана— при 44,1 °С, для этиламина— при 35,7 °С.
Гораздо более высокие давления развиваются при повышении температуры в тех случаях, когда тара заполнена жидкостью полностью, без воздушного пространства. Расчет показывает, что для разрушения даже неповрежденных стеклянных бутылей, заполненных органическими растворителями «под пробку», достаточно повышения температуры всего на 5—10 °С. Для предотвращения подобных явлений при расфасовке жидкостей тару не доливают примерно на 10%.
При замерзании органических жидкостей в стеклянных бутылках, как правило, не происходит их разрушения. Вода и водные растворы в процессе замерзания расширяются и разрушают даже очень прочную тару. Аварии подобного рода особенно опасны тем, что пролив жидкости, может остаться долгое время незамеченным, в результате чего образуется значительный объем взрывоопасной смеси, как это произошло в описанном ниже случае.
.Рабочий ночной смены в цехе химического завода почувствовал сильный запах бензола. Удалось установить, что источник запаха находится в одном из помещений заводской лаборатории, расположенной этажом выше. Начальник смены вместе с работником охраны вскрыли лабораторную комнату, чтобы обнаружить и ликвидировать причину утечки бензола. Пытаясь включить освещение, они ошибочно включили силовой рубильник. В тот же момент в комнате возник пожар, огонь охватил вытяжной шкаф. Несмотря на оперативные действия по-ликвидации пожара, площадь горения стала быстро увеличиваться, и вскоре пламя распространилось на ~~часть помещения. В результате пострадала большая часть мебели и оборудования. .,
В ходе анализа происшествия выяснилось следующее. Работники лаборатории в конце рабочего дня принесли в комнату бутыль с замерзшим бензолом вместимостью 20 л для оттаивания. Бутыль хранилась на складе в плетеной корзине; в той же корзине она была принесена в лабораторию и поставлена в вытяжной шкаф.
Поскольку во время тушения пожара бутыль разбилась, причину ее повреждения, вызвавшего вытекание бензола, удалось установить, только путем сопоставления фактов. Бензол, хранившийся в бутыли, представлял собой отгон водного азеотропа, полученного в цехе. По технологическому журналу удалось установить, что отгон содержал до 7% воды. При хранении образовался слой воды толщиной 4—5 см.
При понижении температуры замерз вначале бензольный слой. Поскольку бутыль была заполнена почти доверху (верхняя, коническая часть бутыли, как показали работники лаборатории, была заполнена на половину высоты), при замерзании нижнего водного слоя за счет. Так как бутыль стояла в корзине, лаборанты не заметили трещины. К моменту возникновения пожара успела оттаять и вытечь только часть бензола. Оставшаяся часть растаяла уже под действием пламени, что и вызвало усиление пожара.
Воспламенение паров бензола, как показала экспертиза, произошло от искры при срабатывании реле сушильного шкафа — бутыль стояла рядом с ним. Сушильный шкаф большой мощности был подключен к распределительному щиту. Тумблер «Сеть» в момент происшествия находился в положении «Вкл». Поэтому привключении общего рубильника сушильный шкаф оказался включенным.
Гораздо труднее оказалось определить степень виновности каждого из участников происшествия. Практика оттаивания-бензола в лабораторном помещении была вызвана необходимостью: склад ЛВЖ не отапливался, и в зимнее время бензол перед расфасовкой приходилось размораживать. Специального помещения для этой цели на заводе не было. Прежде такие операции неоднократно роводились с ведома отдела техники безопасности. Правда, отгон водного азеотропа бензола использовался в лаборатории впервые. С другой стороны, не существует каких-либо правил, запрещающих применение регенерированных растворителей. Действия начальника смены были признаны правильными. Ошибочное включение силового рубильника вряд ли можно поставить ему в вину, так как он не был знаком с расположением выключателей в комнате и действовал в темноте.
Одной из лричин разрушения тары явилось слишком большое количество растворителя в бутыли. Если бы была заполнена только цилиндрическая часть, при замерзании водного слоя масса бензола поднялась бы вверх. Но аппаратчик, заполнявший бутыль, не мог предвидеть, что присутствие водного слоя приведет к таким последствиям. Чистый бензол при том же уровне не разрушает бутыль во время замерзания.
Характерно, что вскоре после происшествия в цехе был оборудо: ванотапливаемый склад ЛВЖ.
При случайном проливе ЛВЖ необходимо принять меры для ликвидации аварийной ситуации в зависимости от конкретных обстоятельств.
При проливе значительных количеств ЛВЖ (более 1 л) следует прежде всего устранить возможность воспламенения паров—обесточить работающее электрооборудование общим рубильником, погасить газовые горелки и спиртовки. В зоне вероятных пожаровзрывоопасных концентраций паров нельзя выключать электроприборы с помощью тумблеров или выдергивания вилки из розетки: в момент прерывания электрической цепи образуется искра, которая может явиться источником зажигания.
Следует помнить, что пары многих органических растворителей весьма токсичны. При проливе за счет большой поверхности испарения быстро создаются высокие концентрации, представляющие опасность для здоровья и~ даже для жизни. В некоторых случаях острые отравления могут возникнуть после 5—10 минут пребывания в отравленной атмосфере или даже после нескольких вдохов, Поэтому ликвидацию пролива значительных количеств токсичных жидкостей необходимо осуществлять в противогазе. Лица, не участвующие в уборке, должны покинуть помещение.
Значительные количества пролитой ЛВЖ, если позволяют обстоятельства, рекомендуется убирать с помощью водоструйного насоса, засасывая жидкость в склянку подобно тому, как это делается при сборе пролитой ртути (см. рис. 92). Остатки ЛВЖ, которые не удается собрать водоструйным насосом, а также небольшие проливы засыпают фильтроперлитовым порошком, мелкими сухими древесными опилками, песком (см. разд. 3.3). После полного впитывания, жидкости массу собирают пластмассовым совком в ведро и выносят в безопасное место для сжигания.
Предотвращение возможности воспламенения
Источниками зажигания паровоздушной смеси могут служить не только открытое пламя и сильно нагретые предметы. Пары ЛВЖ могут воспламеняться также от искр, возникающих при работе исправного электрооборудования, в том числе электромоторов, реле и т. д., от искр, образующихся при падении металлических предметов. Другие источники воспламенения — теплота химических реакций, контакт с каталитически активными материалами, с сильными окислителями. В определенных условиях Источниками воспламенения могут быть искры, возникающие в результате накопления статического электричества.
Поэтому любые работы с ЛВЖ, при которых в окружающее пространство могут выделяться горючие пары, следует проводить при выключенных горелках, электрических приборах и потенциальных источниках зажигания. Чтобы избежать случайного применения пламени или электричества в опасном соседстве с ЛВЖ, следует перед началом работы с пожароопасными веществами поставить об этом в известность всех работающих в данном помещении.
Примерами работ, при которых возможно выделение горючих паров в атмосферу, могут служить экстрагирование веществ с помощью делительных воронок, тонкослойная и бумажная хроматография, работы связанные с необходимбстью переливания ЛВЖ, и др
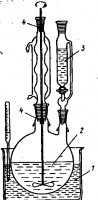
Нагревание ЛВЖ можно производить только в приборах и установках, обеспечивающих полную конденсацию образующихся паров. В качестве нагревательных приборов нельзя использовать электроплитки с открытой "спиралью, а также открытое пламя. При необходимости нагревания ЛВЖ, относящихся к I разряду, особенно диэтилового эфира и сероуглерода, следует либо использовать предварительно нагретые в другом месте жидкостные бани, либо применять бани с погружным нагревательным элементом (см. рис. 21).
Пероксиды в органических растворителях. Образование пероксидов
Скорость образования пероксидов, а также их количество сильно колеблются и зависят от ряда факторов, которые еще недостаточно изучены. Однако не подлежит сомнению, что основные факторы, влияющие на образование пероксидов, это природа растворителя, наличие ингибиторов и условия хранения.
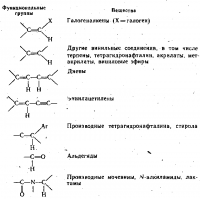
Природа растворителя. При контакте с кислородом воздуха при комнатной температуре пероксиды могут образовываться в веществах, содержащих следующие функциональные группы.
Склонность к образованию пероксидов неодинакова у различных групп соединений. Так, альдегиды и амиды образуют их очень легко, но они быстро разлагаются, и их концентрация не достигает опасного уровня. Исключительно велика способность образовывать перок-сиды у таких соединений, как диизопропиловый эфир, дивинилацетилен, винилиденхлорид. В диизопропило-вом эфире*наличие пероксидов при контакте с воздухом обнаруживается уже через несколько часов после аб-солютирования и перегонки, в тетрагидрофуране — через 3 дня хранения, а в диэтиловом эфире — через 8 дней. По способности реагировать с кислородом воздуха сравнимы с тетрагидрофураном и диэтиловым эфиром диоксан, ацеталь, диметиловый эфир этилен-гликоля (глим), виниловые эфиры, дициклопентадиен, диацетилен, метилацетилен, декагидронафталин (декалин), тетрагидронафталин (тетралин), циклогексан, лиметиловый эсЬио диэтиленгликоля (диглим).
Наличие антиоксидантов (ингибиторов окисления).
Поступающие в продажу растворители и реактивы, способные образовывать пероксиды, содержат антиок-сидант, предотвращающий образование и накопление пероксидов в процессе хранения в закрытых бутылках в течение гарантийного срока. Однако после длительного хранения растворителя проверка на присутствие пероксидов является обязательной. Следует помнить, что антиоксидант лишь увеличивает индукционный период до начала окисления.
В качестве ингибиторов окисления для простых эфиров рекомендуются добавки либо М-бензил-и-ами-нофенола в количестве 15 мг на 1 кг растворителя, либо диэтилентриамина, триэтилентетрамина или тетра-этиленпентамина в количестве 50 г на 1 кг растворителя.. Диэтиловый эфир обычно стабилизируют пирогаллолом, добавляемым в количествах от 1 до 50—200 мг на 1 кг растворителя. Ингибирующим действием в количествах 0,05 мг на 1 кг эфира обладает и диэтилдитио-карбамат натрия, роль которого, по-видимому, заключается в дезактивировании следов металлов, катализирующих окисление.
Образование пероксидов резкб замедляется или полностью прекращается при контакте растворителя с медной сеткой. Наличие воды в эфире замедляет, хотя и не предотвращает полностью образование пероксида. Абсолютный диэтиловый эфир при прочих равных условиях окисляется значительно быстрее, чем эфир, содержащий несколько десятых долей процента воды.
Очистка растворителей, в том числе обработка адсорбентами, осушителями, промывка водой, перегонка, приводит к удалению ингибитора. Поэтому после очистки, если растворитель не используется немедленно, следует либо вновь стабилизировать его добавкой соответствующего ингибитора, либо обеспечить условия хранения, исключающие контакт с воздухом.

Хранение эфиров и других окисляющихся растворителей. Как бы ни была высока способность растворителя образовывать пероксиды, в отсутствие кислорода окисления не происходит. При хранении растворителей на складах в фабричной упаковке необходимо следить за тем, чтобы пробка (или крышка) не была повреждена.
При необходимости длительного хранения иногда целесообразно провести дополнительное парафиниро-вание емкостей с растворителем. В то же время следует иметь в виду, что парафин и полиэтилен, хотя и в незначительной степени, но все же проницаемы для кислорода. Вследствие диффузии кислорода через полиэтиленовые пробки за несколько лет хранения даже в плотно укупоренных емкостях может накопиться значительное количество пероксидов. Суточные колебания температуры в хранилищах способствуют проникновению кислорода в бутылки с растворителями. Днем при повышении температуры пары растворителя расширяются и выходят через неплотности в пробке. При понижении температуры в ночные часы происходит обратный процесс — засасывание воздуха в бутылку.
При отливании растворителя из емкости, в нее попадает сразу значительное количество воздуха, в результате чего процесс образования пероксидов резко ускоряется. После многократного вскрывания емкости можно почти не сомневаться, что оставшийся растворитель будет содержать повышенное количество пероксидов. По этой причине растворители, склонные к образованию пероксидов, недопустимо держать в бутылках большой вместимости —10 или 20 л. В большей степени отвечают требованиям техники безопасности бутылки вместимостью не более 1 л, например для диэтилового эфира максимально безопасна расфасовка в бутылки по 100мл («Эфир для наркоза»). В условиях химической лаборатории такая расфасовка наиболее удобна.
В любом случае не следует оставлять в бутылке небольшое количество легколетучих эфиров. После опорожнения бутылки из-под растворителя, склонного к окислению, ее необходимо ополоснуть водой.
В литературе описан случай сильного взрыва пустой 2-литровой бутылки из-под диэтилового эфира. Взрыв произошел при попытке вынуть заклинившуюся притертую пробку. Очевидно, в бутылке оставалось небольшое количество эфира, который испарился через неплотный шлиф, -в результате чего там сконцентрировался пероксид. При переворачивании бутылки он, вероятно, попал на шлиф. Причиной взрыва послужило трение при вынимании пробки [59].
Нагревание и освещение ускоряют процессы окисления, поэтому растворители, склонные к образованию пероксидов, следует хранить в бутылках из темного стекла и по возможности на холоду.
Особое внимание следует уделять хранению абсолютированных и перегнанных растворителей. Если по каким-либо причинам добавлять антиоксидант в очищенный растворитель недопустимо, лучше всего проводить перегонку непосредственно перед использованием растворителя. В тех случаях, когда очищенный растворитель все же приходится сохранять в течение более или менее длительного времени, необходимо позаботиться о предотвращении его контакта с кислородом воздуха как в процессе хранения, так и при отборе части растворителя из емкости.
Наиболее надежная защита от окисления достигается при хранении растворителя в склянке с тщательно притертой пробкой, смазанной подходящей смазкой, в атмосфере инертного газа. После каждого отливания растворителя емкость обязательно заново продувают инертным газом.
При необходимости многократного отбора небольших порций абсолютированного растворителя рекомендуется хранить его в сосуде Шлепка в атмосфере сухого азота или аргона (рис. 58). Чтобы избежать переливания растворителя на воздухе, перегонку производят непосредственно в сосуд Шленка, из которого затем вытесняют воздух инертным газом. При отборе растворителя необходимое его количество выдавливают через боковой градуированный отвод током инертного газа.
Обнаружение пероксидов
Прежде чем приступить к перегонке эфира или другого способного окисляться растворителя, следует убедиться в отсутствии в нем пероксидных соединений. Проведение теста на наличие пероксидов обязательно перед использованием растворителя для экстракции или других целей, если в дальнейшем предполагается его упаривание, а также при работе с соединениями, способными вступать в реакции по радикальному механизму.
Удаление пероксидов
Адсорбция оксидом алюминия. Хорошим адсорбентом для удаления пероксидовиз органических растворителей служит активированный оксид алюминия. Имеющийся в продаже оксид алюминия для хроматографии первой или "второй степени активности пригоден для использования без дополнительного прокаливания. Если необходимо активировать оксид алюминия, его прокаливают в течение 6 ч при 300-400°С.
Для удаления пероксидов растворитель выдерживают в течение суток над оксидом алюминия. Применение перемешивания позволяет сократить время обработки до 1 — 1,5 ч. Еще быстрее можно освободиться от пероксида, пропустив растворитель через стеклянную колонку, заполненную оксидом алюминия.
Оксид алюминия не разрушает, а лишь адсорбирует пероксиды, поэтому сразу после обработки растворителя следует, не дожидаясь высыхания адсорбента, чалить его 5 % оаствооом РеБО.». Можно элюировать адсорбированный пероксид горячей водой или метанолом.
После обработки следует убедиться в отсутствии пероксида в растворителе, повторив один из предложенных выше тестов.
Метод пригоден для извлечения пероксидов из любых растворителей, в том числе смешивающихся с водой, например диоксана. Одновременно происходит осушка и очистка растворителей, особенно от примесей кислотного характера.
Обработка ионообменной смолой. Это простой и надежный метод удаления пероксидов из эфиров и других растворителей высокой чистоты без перегонки и потери растворителя. Так, в эксперименте с помощью колонки диаметром 10 мм, содержащей 4 г анионообменной смолы, полностью удалили пероксид из 2-литровой бутыли с диэтиловым эфиром, предварительно содержавшимся при доступе воздуха в течение 3 месяцев.
Экстракция концентрированным раствором щелочи. Этим методом могут быть экстрагированы пероксиды из эфиров, нерастворимых или малорастворимых.в воде. Так, при перемешивании в течение 0,5 ч 1 об. ч. 23% №ОН с 10 об. ч. диэтилового эфира пероксиды полностью гидролизуются. Следует иметь в виду, что некоторые пероксиды, например ди-тргг-бутилпероксид, устойчивы к гидролизу.
Обработка . водными растворами неорганически* восстановителей. Этот способ позволяет быстро удалить пероксиды из эфиров, не смешивающихся с водой. Наибольшее распространение получили растворы сульфата железа (II), метабисульфита натрия Ыа25205, сульфида натрия. Сульфат железа(П) используют в виде 30%-го раствора в количестве 10—15 мл на 1 л эфира. Пероксиды полностью удаляются при встряхивании эфира с раствором восстановителя в делительной воронке в течение 3—5 мин.
Примечание. Обработка гранулированной щелочью в твердом виде, как правило, не приводит к удалению пероксида даже при кипячении растворителя. Распространенное мнение, что в хранящемся над гранулированной щелочью растворителе не образуются пероксиды, ошибочно.
Вернуться назад